
Micro-PA aktywuje hipertrofię

Mięsień. Spędzamy niezliczone godziny, wciskając żelazo, aby upakować go więcej na naszych ciałach. Koncentrujemy naszą dietę na jej odżywianiu i karmieniu. Ciągle szukamy sposobów na lepsze i szybsze zyski.
Dla większości z nas podnoszenie ciężarów to nie tylko hobby czy po prostu coś, co robimy, to w dużej mierze część naszej tożsamości. W rzeczywistości prawdopodobnie spędzamy więcej czasu na myśleniu o stymulowaniu wzrostu mięśni, niż większość z nas chciałaby przyznać, i zawsze szukamy najnowszych wiadomości o hipertrofii.
Jeśli to ty, mam pewne informacje, które nie tylko rozświetlą synapsy twojego mózgu. Niektóre z nich są trochę geekowe i techniczne, ale są również bardzo ważne i zapewniają jaśniejszy, bardziej skoncentrowany obraz tego, co jest zaangażowane w budowanie mięśni.
Oto, co musisz wiedzieć…
- Trening siłowy powoduje wzrost mięśni poprzez aktywację mTOR, który jest głównym enzymem odpowiedzialnym za syntezę białek komórek mięśniowych, co prowadzi do hipertrofii.
- Komórki mięśniowe podczas ekscentrycznych skurczów wytwarzają kwas fosfatydowy (PA), który aktywuje mTOR.
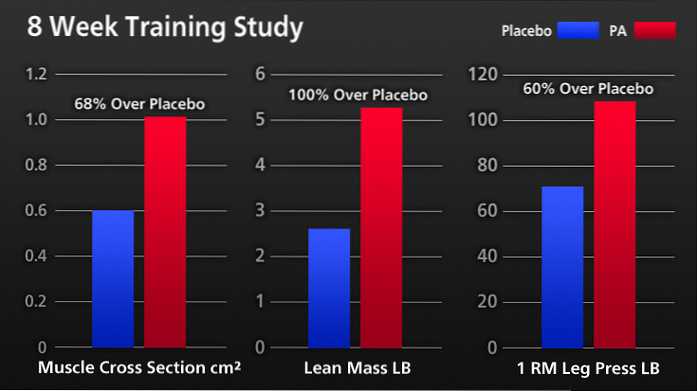
- Osoby przyjmujące suplement PA osiągnęły o 50% większy wzrost pola przekroju mięśniowego i beztłuszczowej masy ciała, 40% większy wzrost całkowitej siły (górnej i dolnej części ciała) oraz 60% większą utratę tkanki tłuszczowej niż grupa tylko treningowa ( Wilson i in. 2014, w druku).
- Inne badanie, w którym wzięli udział mężczyźni wytrenowani siłowo, przechodzący 8-tygodniowy program ćwiczeń, wykazało, że osoby przyjmujące 750 mg PA dziennie zyskały znacznie więcej beztłuszczowej masy ciała i siły niż grupa wyłącznie treningowa (Hoffman et al. 2013).
- Micro-PA zawiera wysoce wyspecjalizowaną formę kwasu fosfatydowego (PA), który silnie aktywuje i wzmacnia syntezę białek mięśniowych.
Nowa nauka o hipertrofii
Wykonując serię powtórzeń pod obciążeniem, twoje ciało zaczyna przekształcać informacje mechaniczne w działanie biochemiczne. Określenie to nazywa się mechanotransdukcja i stanowi podstawę najsilniejszego bodźca wewnątrzkomórkowej syntezy białek (inaczej hipertrofii).
Oto dokładnie, jak to działa. Podczas ekscentrycznego ruchu enzym jest usuwany z linii Z komórek mięśniowych, który hydrolizuje fosfatydylocholinę do kwasu fosfatydowego (PA). PA z kolei wiąże się i aktywuje enzym kinazę, zwany mTOR, który jest „głównym regulatorem” syntezy białek komórek mięśniowych i wielkości mięśni.
Aktywowany PA mTOR bezpośrednio wpływa na natychmiastowe i długotrwałe zmiany we wzroście mięśni. Mówiąc najprościej, jeśli chcesz nabrać mięśni, musisz aktywować mTOR. Im więcej PA jest dostępne do aktywacji mTOR, tym większy wpływ na syntezę białek wewnątrzkomórkowych i większy przyrost masy mięśniowej.
Podsumowanie badań PA
- Wiele badań wykazało, że PA aktywuje i wzmacnia „główny enzym regulacyjny” odpowiedzialny za natychmiastowe i długotrwałe zmiany we wzroście mięśni (inaczej syntezę białek).
- PA kąpane in vitro z mioblastami (komórkami mięśni młodych) spowodowało 8-krotny wzrost aktywacji mTOR.
- PA bezpośrednio zwiększa syntezę białek, wchodząc do komórki mięśniowej i wiążąc się z mTOR.
- PA zwiększa syntezę białek pośrednio, przekształcając się w kwas lizofosfatydowy i przyłączając się do błony komórkowej mięśni, co zwiększa wewnątrzkomórkowy PA, a z kolei aktywuje mTOR.
- Biodostępność PA znacznie wzrasta w ciągu 30 minut i pozostaje podwyższona przez 7 godzin.
- Badanie, w którym wzięli udział mężczyźni trenujący oporowo, przechodzący bardzo intensywny program ćwiczeń, wykazało, że osoby suplementujące 750 mg PA dziennie osiągnęły:
50% większy wzrost pola przekroju mięśniowego i beztłuszczowej masy ciała.
40% większy wzrost całkowitej siły (górna i dolna część ciała)
60% większa utrata tkanki tłuszczowej niż w grupie tylko treningowej (Wilson i in. 2014, w druku).
- Inne badanie, w którym wzięli udział mężczyźni wytrenowani siłowo, przechodzący 8-tygodniowy program ćwiczeń, wykazało, że osoby przyjmujące 750 mg PA dziennie zyskały znacznie więcej beztłuszczowej masy ciała i siły niż grupa wyłącznie treningowa (Hoffman et al. 2013):
Forum dzienników i użytkowników Micro-PA ™
Obecnie współpracujemy z Christianem Thibaudeau, profesjonalistami IFBB Markiem Dugdale'em i Amitem Sapirem, a także kilkoma innymi czołowymi sportowcami, testując i udoskonalając techniki treningowe, aby czerpać jak największe korzyści z Micro-PA.™ Możesz sobie wyobrazić, jak trudno jest wzmocnić mięśnie tych, którzy są już u szczytu kariery, ale wyniki są imponujące. Wszystko, co robimy, jest publikowane i omawiane na forum Micro-PA Logs & Users . Jeśli więc jesteś użytkownikiem Micro-PA lub po prostu chcesz zobaczyć, co mówią i robią profesjonaliści, sprawdź to.
Jako poważny zawodnik już ciężko trenujesz. Teraz nadszedł czas, aby zwiększyć wyniki swoich wysiłków. Micro-PA ™ nie tylko zapewnia przewagę na siłowni. Bezpośrednio aktywuje i wzmacnia hipertrofię. To nie jest hobby. A Micro-PA ™ nie jest dla tych, którzy traktują go jak jeden.
Protokół treningu Micro-PA ™
| Harmonogram | Suplement | Instrukcje dotyczące dawkowania |
| 01:00 Przed treningiem | Micro-PA ™ | 6 kapsułek |
| 00:30 Przed treningiem | Indigo-3G® | 6 kapsułek |
| 00:15 Przed treningiem | Plazma ™ | Dawka 500 ml |
| Trening | Plazma ™ | 3 lub 4 dawki (po 500 ml). Spożywać w pulsach o połowę, równomiernie rozłożonych w czasie trwania treningu. |
| 00:00 - 01:00 Po treningu | Mag-10® | 2 dawki (po 500 ml). Spożywać obie dawki w ciągu godziny po treningu. |

Bibliografia
- Gundermann, D i in. Kwas fosfatydowy pochodzenia sojowego, kwas lizofosfatydowy i fosfatydyloseryna są wystarczające, aby wywołać wzrost sygnalizacji mTOR. Plakat zaprezentowany na dorocznej konferencji ISSN w 2013 r., A rękopis jest obecnie recenzowany w celu przesłania do publikacji.
- Hoffman, JR i in. Skuteczność spożycia kwasu fosfatydowego na beztłuszczową masę ciała, grubość mięśni i przyrost siły u mężczyzn po treningu oporowym. Dziennik Międzynarodowego Towarzystwa Żywienia Sportowego. 9:47 2012.
- Joy, JM i in. Suplementacja kwasu fosfatydowego zwiększa przerost i siłę mięśni szkieletowych. Plakat zaprezentowany na dorocznej konferencji ISSN w 2013 r., A rękopis jest obecnie recenzowany w celu przesłania do publikacji.
- Joy, JM i in. Wpływ 8 tygodni suplementacji kwasem fosfatydowym na bezpieczeństwo układu sercowo-naczyniowego, nerek i wątroby w zdrowiu młodych mężczyzn. Plakat zaprezentowany na dorocznej konferencji ISSN 2013.
- Purpura M i in. Wpływ doustnego podawania kwasu fosfatydowego pochodzącego z soi na stężenie kwasu fosfatydowego i gatunków molekularnych kwasu lizofosfatydowego w ludzkim osoczu. Plakat zaprezentowany na dorocznej konferencji ISSN 2013.
- Adegoke, OA, Abdullahi, A, Tavajohi-Fini, P. mTORC1 oraz regulacja anabolizmu i masy mięśni szkieletowych. Fizjologia stosowana, odżywianie i metabolizm. Vol. 37, nie. 3: 395-406, 2012.
- Donati C, i in. Nowe spojrzenie na rolę 1-fosforanu sfingozyny i kwasu lizofosfatydowego w regulacji biologii komórek mięśni szkieletowych. Biochimica et Biophysica Acta, 2012, http: // dx.doi.org / 10.1016 / j.bbalip.2012.06.013.
- Foster, D i in. Kwas fosfatydowy i wykrywanie lipidów przez mTOR. Artykuły z prasy komórkowej w prasie, Trendy w endokrynologii i METABOLIZM XX (2012) 1-7.
- Harrington, LS, Findlay, GM i Lamb, RF. Ograniczanie PI3K: sygnalizacja mTOR wraca do membrany. TRENDY w Biochem Sci 30 (1): 35-42, 2005.
- Hornberger, TA, Chu, WK, Mak, YW, Hsiung, JW, Huang, SA i Chien, S. Rola fosfolipazy D i kwasu fosfatydowego w mechanicznej aktywacji sygnalizacji mTOR w mięśniach szkieletowych. PNAS 103 (12): 4741-4746, 2006.
- Hornberger, TA, Sukhija, KB, Chien, S. Regulacja mTOR przez mechanicznie indukowane zdarzenia sygnalizacyjne w mięśniach szkieletowych. Cell Cycle 5 (13): 1391-1396, 2006.
- Hulmi JJ i in. Ćwiczenia oporowe ze spożyciem białka serwatki wpływają na szlak sygnałowy mTOR i miostatynę u mężczyzn. J Appl Physiol 106: 1720-1729, 2009.
- Laplante M i in. Wyłaniająca się rola mTOR w biosyntezie lipidów. Current Biology 19, R1046-R1052, 1 grudnia 2009. Elsevier Ltd.
- Lehman, N, Ledford, B, Di Fulvio, M, Frondorf, K, McPhail, LC i Gomez-Cambronero, J. Kwas fosfatydowy pochodzący z fosfolipazy D2 wiąże się z rybosomalną kinazą p70 S6 i aktywuje ją niezależnie od mTOR. FASEB J 21: 1075-1087, 2007.
- O'Neil, TK, Duffy, LR, Frey, JW i Hornberger, TA. Rola 3-kinazy fosfoinozytydu i kwasu fosfatydowego w regulacji ssaczego celu rapamycyny po ekscentrycznych skurczach. J Physiol 581.14: 3691-3701, 2009.
- Rasmussen, BB. Kwas fosfatydowy: nowatorski mechanizm mechaniczny, w jaki sposób ćwiczenia oporowe aktywują sygnalizację mTORC1. J Physiol 587.14: 3415-3416, 2009.
- Sengupta, S, Peterson, TR i Sabatini, DM. Regulacja szlaku kompleksu 1 mTOR przez składniki odżywcze, czynniki wzrostu i stres. Molecular Cell 40: 310-322, 2010.
- Stipp D. Nowa droga do długowieczności. Scientific American, styczeń 2012.
- Veverka, V, Crabbe, T, Bird, I, Lennie, G, Muskett, FW, Taylor, RJ i Carr, MD. Charakterystyka strukturalna interakcji mTOR z kwasem fosfatydowym i nową klasą inhibitorów: przekonujące dowody na centralną rolę domeny FRB w regulacji mTOR za pośrednictwem małych cząsteczek. Oncogene 27: 585–595, 2008.
- Vissing K i in. Zróżnicowana sygnalizacja mTOR, ale nie AMPK po ćwiczeniach siłowych vs wytrzymałościowych u osób przyzwyczajonych do treningu. Scand J Med Sci Sports, 2011, doi 10.1111 / j.1600-0838.2011.01395.x.
- Walker, DK, Dickinson, JM, Timmerman, KL, Drummond, MJ, Reidy, PT, Fry, CS, Gundermann, DM i Rasmussen, BB. Ćwiczenia, aminokwasy i starzenie się w kontroli syntezy białek mięśni ludzkich. J Am Coll Sport Med 43 (12): 2249-2258, 2011.
- Winter, JN, Fox, TE, Kester, M, Jefferson, LS i Kimball, SR. Kwas fosfatydowy pośredniczy w aktywacji mTORC1 poprzez szlak sygnałowy ERK. Am J Physiol Celi Physiol 299: C335-C344, 2010.
- Xu, Y, Fang, Y, Chen, J i Prestwich, GD. Aktywacja sygnalizacji mTOR przez nowe analogi fluorometylenofosfonianowe kwasu fosfatydowego. Bio Med Chem Letter 14: 1461–1464, 2004.
- Yamada, AK, Verlengia, R, Bueno, CR. Szlaki mechanotransdukcji w przerostach mięśni szkieletowych. Journal of Receptors and Signal Transduction 2011.
- Zanchi, NE i Lancha, AH Jr. Mechaniczne bodźce mięśni szkieletowych: wpływ na syntezę mTOR / p70s6k i białek. Eur J Appl Physiol 102: 253-263, 2008.
- Zhang C i in. Sygnały glicerolipidowe zmieniają kompleks mTOR 2 (mTORC2) w celu osłabienia sygnalizacji insuliny. PNAS Early Edition, www.pnas.org / content / early / 2012/01/10/1110730109.pełny.pdf.



Jeszcze bez komentarzy